Los retos de la edición genética
El uso de técnicas capaces de editar y modificar genes humanos está salvando vidas, pero también plantea cuestiones éticas que algunos investigadores ya han ignorado y cuyas consecuencias pueden ser dramáticas.
Artículo
Si quieres apoyar el periodismo de calidad y comprometido puedes hacerte socio de Ethic y recibir en tu casa los 4 números en papel que editamos al año a partir de una cuota mínima de 30 euros, (IVA y gastos de envío a ESPAÑA incluidos).
COLABORA2023
Artículo
Érase una vez tres niñas que se hicieron mundialmente famosas sin haber destacado en ninguna disciplina ni haber contribuido de manera milagrosa a algún avance científico. Su fama, en realidad, no tenía que ver con ellas, ya que provenía de algo que les ocurrió incluso antes de nacer; algo sobre lo que ellas, obviamente, no tuvieron capacidad de decisión.
A finales de 2018, así, el mundo asistía atónito a las noticias sobre un investigador chino que había editado genéticamente embriones humanos de los que habían nacido tres niñas por fertilización in vitro. No fueron pocas las voces que se alzaron contra un experimento de ecos eugenésicos: la comunidad científica internacional, de forma casi unánime, condenó la irresponsabilidad y falta de ética de He Jiankui, que se defendió aduciendo que su intención era generar seres humanos resistentes a una infección por VIH.
Y aunque así comenzó todo, del final poco sabemos: Jiankui fue condenado a prisión por el Gobierno chino y de las tres niñas nada se sabe, ya que el mismo Gobierno no facilita información alguna, amparándose en el respeto a la privacidad. Lo que sí conocemos son parte de los escenarios en que se ha desarrollado esta extraordinaria fábula real.
Los 300.000 bebés que nacen cada año con anemia de células falciformes podrían tener una vida sana gracias a la edición genética
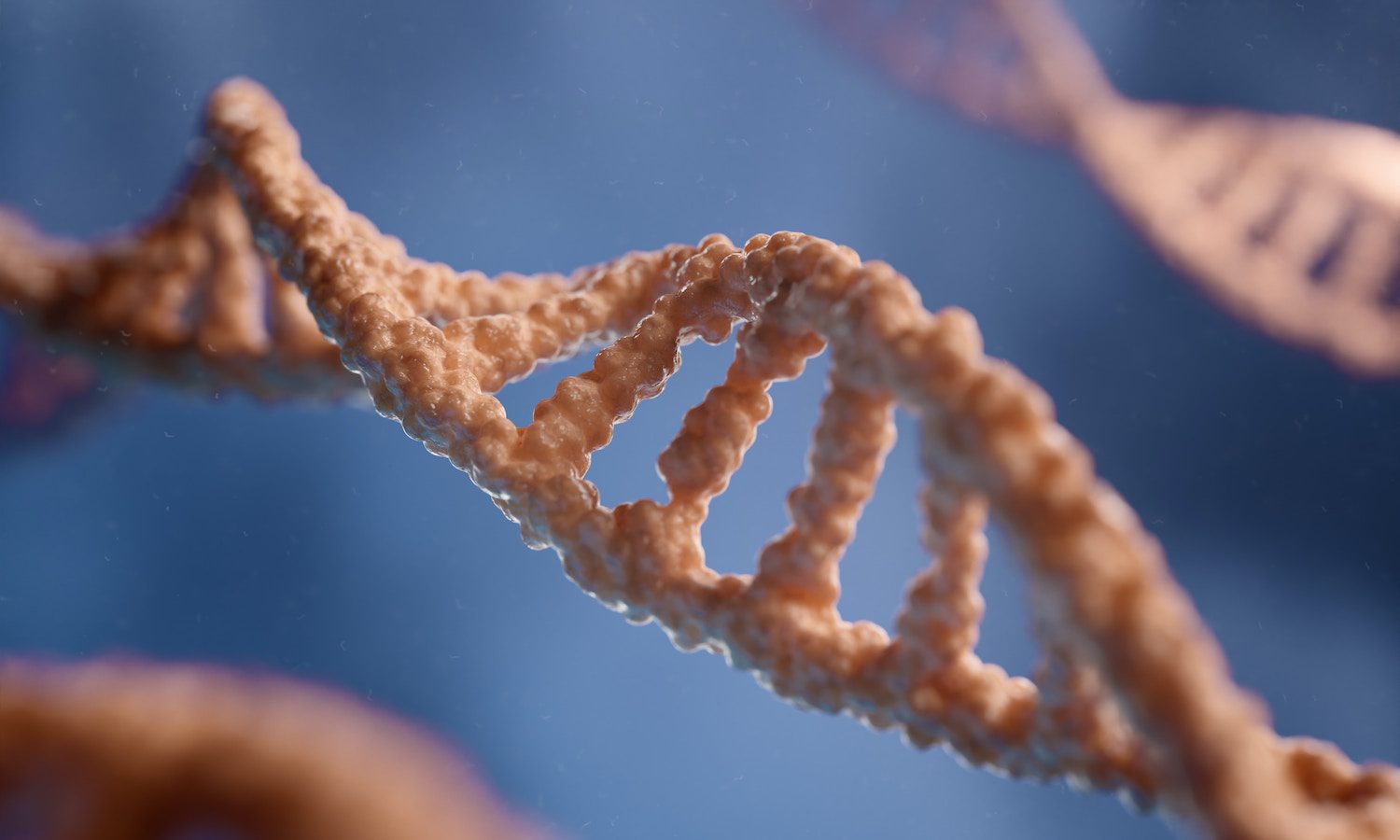
La herramienta que utilizó Jianku para llevar a cabo su «hazaña» se llama CRISPR (acrónimo en inglés, de Repeticiones Palindrómicas Cortas Agrupadas y Regularmente Espaciadas), y lo que logra es cortar y pegar el ADN. Esta técnica comenzó a desarrollarse a partir de 2005, abriendo un sinfín de perspectivas y posibilidades en el campo de la edición genética.
La tecnología CRISPR funciona con la creación previa de un ARN (la molécula que permite que la información genética que contiene el ADN sea comprendida por las células) coincidente con la pieza de ADN que se pretende modificar. A posteriori, este ARN guía a las enzimas Cas9, una especie de tijeras moleculares que cortan y modifican secciones de ADN asociados a alguna enfermedad. Las Cas9 seccionan la secuencia que les especifica la ARN guía y, a partir de ahí, se abren tres posibilidades: silenciar el gen que no interesa, repararlo con un fragmento de ADN modificado o, incluso, editarlo injertando nuevo ADN. Algo así hizo Jianku con los embriones de las tres niñas.
¿Una técnica para el futuro?
Dejando de lado el mencionado caso, la edición genética está logrando importantes avances en la curación de enfermedades que, hasta ahora, se consideraban inatacables.
Un reciente caso de éxito en el uso del CRISPR es el de la estadounidense Victoria Gray, que sufría anemia de células falciformes, una enfermedad genética con la que nacen cerca 300.000 bebés cada año. En 2019, Gray se convertía en la primera paciente con esta dolencia que recibía una terapia basada en la edición genética. Se extrajeron células madre de su médula ósea y se inhabilitó el gen que provocaba su enfermedad. A posteriori, se mataron todas las células enfermas con quimioterapia, y se le hizo una transfusión con las células editadas con CRISPR. Sólo hicieron falta unas semanas para que una nueva generación de células sanas se multiplicaran por el organismo de la paciente. 4 años después, Gray lleva una vida sana, como ella misma explicó en marzo de este año en el III Congreso Internacional de Edición del Genoma Humano.
Actualmente, varios fármacos que utilizan esta tecnología para acabar con enfermedades genéticas esperan ser aprobados en Estados Unidos.
Pero la técnica CRISPR tiene aplicaciones más allá de nuestra salud. La edición genética se puede utilizar para producir plantas que se adapten mejor a determinados ecosistemas, o especies animales que resistan enfermedades. También para intervenir sobre los ecosistemas, aunque hay que tener la máxima precaución para no provocar daños incontrolables. Idéntica o más precaución hay que tener en el caso del empleo de CRISPR en humanos. La comunidad científica internacional coincide en que sólo debe emplearse en patologías para las que no exista ningún tratamiento efectivo.
La prueba de los riesgos que plantea traspasar la frontera de la ética está en las numerosas ofertas de empleo en países que carecen de regulación a este respecto que ha recibido He Jianku, que aún permanece encarcelado en su país. El caso de las tres niñas chinas es inaceptable desde el punto de vista ético. Editar embriones genéticamente no es un objetivo terapéutico y, como señalan muchos expertos, cualquier avance médico debería ir exclusivamente en esa línea.











COMENTARIOS